

| News Links Veranstaltungen Anreise Kontakt | |
Analyse des Herz-Kreislauf-Systems genetisch veränderter MäuseÜberblickMitarbeiter Publikationen Die zunehmende Zahl genetisch veränderter Mäuse macht es notwendig, daß neben der Molekularbiologie und Genetik auch die Physiologie dieser Tiere aufgeklärt wird. Wir haben deshalb ein Methodenspektrum etabliert, mit dem es möglich ist, kreislaufrelevante Funktionssysteme zu charakterisieren. Wir beschreiben die Nierenfunktion (glomeruläre Filtrationsrate, renale Durchblutung, Natrium- und Wasserausscheidung) und die Herzfunktion (Arbeitsdiagramm des Herzens). Wir charakterisieren auch Schlag zu Schlag Änderungen von Herzfrequenz und Blutdruck (Hering, Traube und Mayer-Wellen), indem wir an nicht-narkotisierten Mäusen mit Hilfe der Fourieranalyse Frequenzspektren der Herzfrequenzvariabilität und der Blutdruckvariabilität erfassen. Die Baroreflexkontrolle der Herzfrequenz wird mittels Kross-Spektralanalyse bewertet. Diese Methoden wurden von der Anwendung am Menschen an das Tiermodell angepasst. Weiterhin haben wir kürzlich die Schlagvolumen- und Herzvolumenmessung in Verbindung mit der telemetrischen Blutdruckmessung an frei beweglichen Tieren eingeführt (Abb.1), und sind damit in der Lage, die systemische Hämodynamik bei diesen Tieren zu beschreiben. Ausserdem haben wir die Methode der direkten Messung der renalen sympathischen Nervenaktivität zur Bestimmung der Baroreflex Kontrolle des Vasomotorentonus bei der Maus etabliert (Abb.2). Zur Zeit liegt unser Schwerpunkt auf der Herz-Kreislauf Analyse von Mäusen, bei denen das RGS2-Gen deletiert wurde.
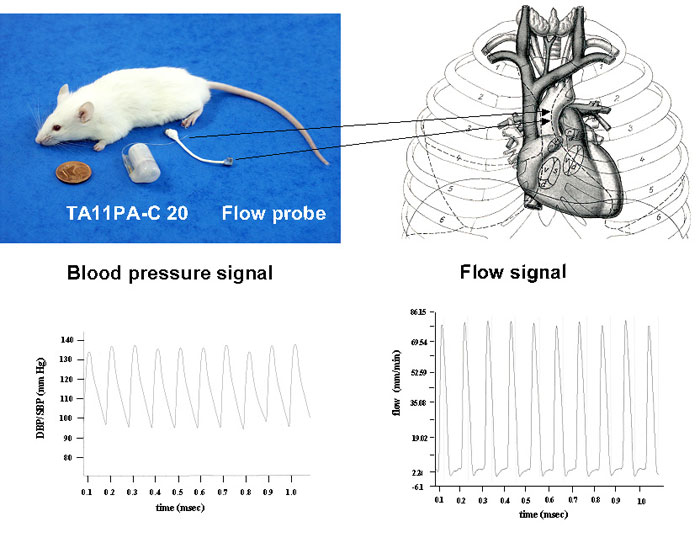 Abb.1 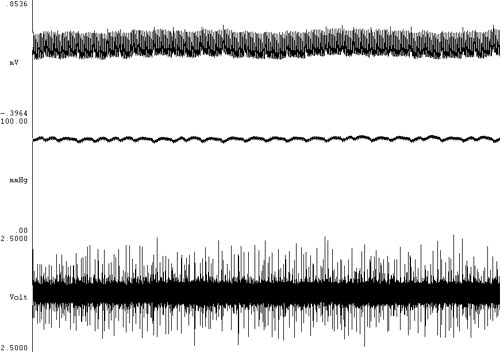 Abb.2: Originalregistrierung von EKG (oben), arteriellem Blutdruck (Mitte) und renaler Nervenaktivität (unten) an der narkotisierten Maus. 
Mitarbeiter:

Publikationen AG Vaskul�re MedizinMolekulare Mechanismen bei Ang II-/Hypertonie-bedingten Nieren-, Herz- und Gef��sch�den. Rolle des Immunsystems.Untersuchung der Rolle von AT1 Rezeptor-Autoantik�rpern bei Pr�eklampsie. Der Einfluss des Transkriptionsfaktors NF-κB auf die Organsch�digung. Der Einfluss von Aldosteron auf die Organsch�digung. Angiotensin II-induzierte Entz�ndungsreaktionen und ihre Kontrolle durch P450-abh�ngige Metabolite mehrfach unges�ttigter Fetts�uren. Dominik N. M�ller (Helmholtz-Stipendiat), Anette Fiebeler, Ralf Dechend Kooperation Nephrologie-Kardiologie
Ziele: 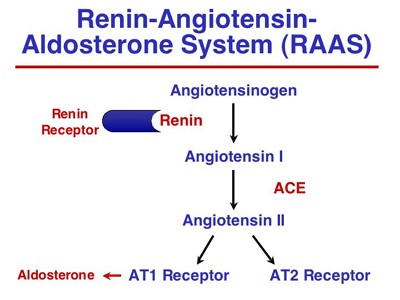 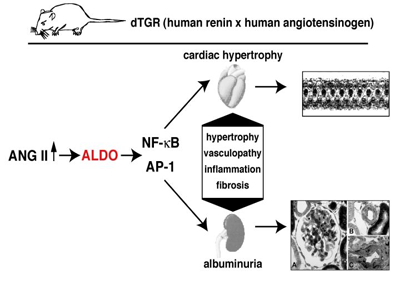  Molekulare Mechanismen bei Ang II-/Hypertonie-bedingten Nieren-, Herz- und Gef��sch�den. Rolle des Immunsystems. Project Leaders: D. N. M�ller, A. Fiebeler, R. Dechend, E. Shagdarsuren, M. Wellner Funding: EuReGene-grant In diesem Projekt soll die Rolle von CD4/CD8 T-Zellen, B-Zellen und dendritischen Zellen bei der Entstehung von Gef��-, Nieren- und Herzsch�den untersucht werden. 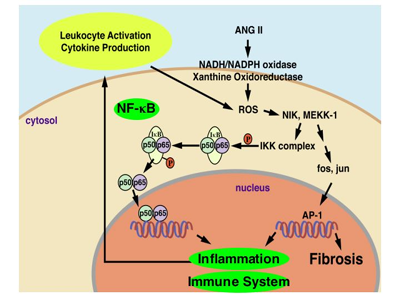 M�ller DN, Shagdarsuren E, Park J-K, Dechend R, Mervaala E, Hampich F, Fiebeler A, Ju X, Finkenberg P, Theuer J, Viedt C, Kreuzer J, Heidecke H, Haller H, Zenke M, Luft FC. Immunosuppressive treatment protects against angiotensin II-induced renal damage. J Am J Pathol 2002;161:1679-1693. Wellner M, Dechend R, Park JK, Shagdasuren E, Al-Saadi N, Kirsch T, Gratze P, Schneider W, Meiners S, Fiebeler A, Haller H, Luft FC, Muller DN. Cardiac Gene Expression Profile in Rats with Terminal Heart Failure and Cachexia. Physiol Genomics. 2004 Dec 28; [Epub ahead of print].  Untersuchung der Rolle von AT1 Rezeptor-Autoantik�rpern bei Pr�eklampsie. Project Leaders: D. N. M�ller, R. Dechend, P. Gratze Collaboration with G. Wallukat, Max-Delbr�ck Center, Berlin and D. Dragun, Charité, Berlin Anhand fr�herer Experimente konnten wir zeigen, dass pr�eklamptische Frauen und manche Patienten mit maligner Hypertonie agonistische Autoantik�rper bilden, die gegen den Ang-II-Rezeptor (AT1) gerichtet sind. Ferner konnten wir feststellen, dass die Antik�rper �ber die Transkriptionsfaktoren NF-kB und AP-1 bei glatten Muskelzellen die Gewebefaktor-Produktion einleiten k�nnen. Vor kurzen haben wir zeigen k�nnen, dass die Antik�rper auch die NADPH-Oxidase stimulieren und zur Produktion von reaktiven Sauerstoffspezien f�hren k�nnen. Wir haben vor Kurzem gezeigt, da� bei einem experimentellen Ratten-Tiermodell es w�hrend der Schwangerschaft sowohl zu einem Blutdruckanstieg mit Albuminurie kommt, als auch AT1 Rezptorantik�rper auftreten Diese Ver�nderungen treten auch bei Pr�eklampsiepatientinnen auf. Diese Tiermodell gibt uns die Gelegenheit die direkte Rolle der Antik�rper als pathogenetischer Mechanismus nachzuweisen. 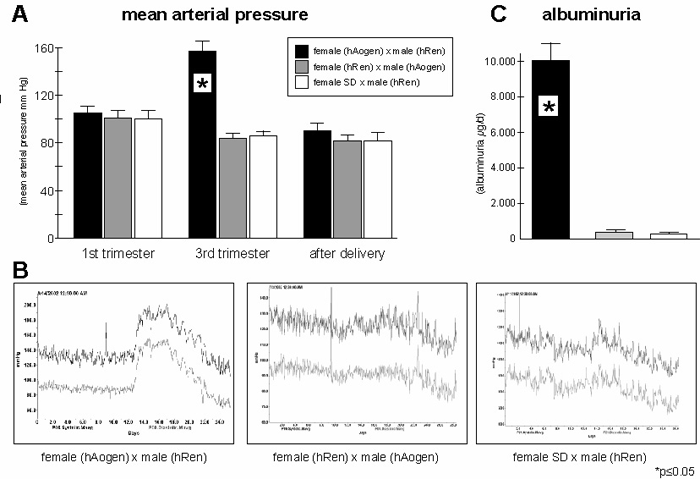 Wallukat G, Homuth V, Fischer T, Lindschau C, Horstkamp B, Jupner A, Baur E, Nissen E, Vetter K, Neichel D, Dudenhausen JW, Haller H, Luft FC. Patients with preeclampsia develop agonistic autoantibodies against the angiotensin AT1 receptor. J Clin Invest 1999;103:945-52. Dechend R, Viedt C, M�ller DN*, Wallukat G, Park J-K, Theuer J, Barta P, Homuth V, Fiebeler A, Kreuzer J, Dietz R, Haller H, Luft FC. AT1 receptor agonist antibodies from preeclamptic patients stimulate NADPH oxidase. Circulation 2003;107(12):1632-9. Dechend R, Gratze P, Wallukat G, Erdenechimeg S, Br�sen J-H, Schneider W, Fiebeler A, Plehm R, Caluwaerts S, Vercruysse L, Pijnenborg R, Luft FC, M�ller DN: Agonistic autoantibodies to the AT1 receptor in a transgenic rat model of preeclampsia. Hypertension 2005;45(4):742-6. Dragun D, M�ller DN, Br�sen H-H, Fritsche L, Nieminen-Kelh� M, Dechend R, Kintscher U, Rudolph B, Hoebeke J, Eckert D, Mazak I, Plehm R, Sch�nemann C, Unger T, Budde K, Neumayer H-H, Luft, FC, Wallukat G: Angiotensin II Type 1-receptor activating antibodies in renal-allograft rejection. N Engl J Med 2005;352:558-69.  Der Einfluss des Transkriptionsfaktors NF-κB auf die Organsch�digung. Project Leaders: D. N. M�ller, R. Dechend, N. Henke Collaboration with R. Schmidt-Ullrich and C. Scheidereit, Max-Delbr�ck Center, Berlin Der nukle�re Transkriptionsfaktor NF-κB ist der wichtigste Regulator von Entz�ndungsreaktionen, Proliferation und Anti-Apoptose. Obwohl eine urs�chliche Beteiligung von NF-κB an der Entstehung von Arteriosklerose und von Hypertonie-bedingtem Endorganschaden von vielen Arbeitsgruppen postuliert wird, gibt es lediglich indirekte Hinweise f�r eine Bedeutung von NF-κB. Der Ansatz unseres Projektes ist es, einen kausalen Zusammenhang zwischen NF-κB-Aktivit�t und der Entstehung von Arteriosklerose und Hypertonie herzustellen. Da NF-κB-Knock-out M�use einen letalen Ph�notyp in der Embryonalphase zeigen, hat Ruth Schmidt Ullrich aus der Arbeitsgruppe von Dr. Claus Scheidereit mittels konditionellem Gen-Targeting ein besonderes, nicht-letales Maus-Modell etabliert. Sie hat durch die transgene �berexpression einer transdominant�positiven Mutante des IKBa (IKB?N) eine Maus hergestellt, bei der die NF-κB-Aktivit�t reduziert ist, ohne dass daraus ein letaler Ph�notyp resultiert. Mittels konditionellem Gen-Targeting mit der Cre-LoxP-Technologie wurde in gemeinsamen Vorarbeiten eine zelltypspezifische NF-κB-Inaktivierung herbeigef�hrt: in unserem Fall wurde eine selektive NF-κB-Inaktivierung in Endothel- und glatten Muskelzellen erzielt. Ziel des Projektes ist es, in den verschiedenen M�usen den kardiovaskul�ren Endorganschaden bei Hypertonie und die Arteriogenese zu untersuchen, wenn die NF-kB Aktivit�t in Endothel- bzw. glatten Muskelzellen in-vivo reduziert ist. Unsere Hypothese ist, dass durch die Reduktion der NF-kB Aktivit�t in vivo, der kardiovaskul�re Endorganschaden bei Hypertonie und Arteriosklerose reduziert ist. Dabei soll ebenfalls untersucht werden, ob die Endothelzelle oder die glatte Muskelzelle der prim�re Ausgangspunkt der pathologischen Gef��reaktion sind. Die Signaltransduktionswege in Endothel- und glatten Muskelzellen der IkB?N M�use sollen untersucht werden, insbesondere in Bezug auf die Proliferation. 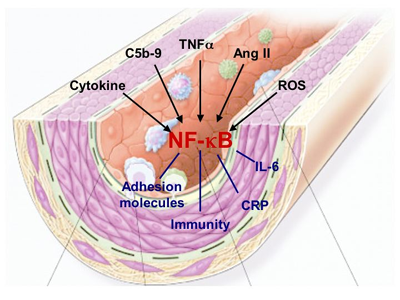 M�ller DN, Dechend R, Mervaala EMA, Schmidt F, Park J-K, Fiebeler A, Theuer J, Breu V, Ganten D, Haller H, Luft FC. NF- κB inhibition ameliorates angiotensin II-induced inflammatory damage in rats. Hypertension 2000;35.193-201. M�ller DN, Heissmeyer V, Dechend R, Hampich F, Park J-K, Fiebeler A, Shagdarsuren E, Theuer J, Elger M, Pilz B, Breu V, Schroer K, Ganten D, Dietz R, Haller H, Scheidereit C, Luft FC: Aspirin inhibits NF-κ B and protects from angiotensin II-induced organ damage. FASEB J 2001; 15: 1822-24.  Der Einfluss von Aldosteron auf die Organsch�digung. Project Leaders: D. N. M�ller, A. Fiebeler Funding: Nationales Genom-Netzwerk NGFN-2 In gro�en klinischen Studien konnte gezeigt werden, dass die Blockade vom Aldosteron (Ald) neben der Ang II Blockade bei Patienten mit isch�mischer Herzerkrankung einen zus�tzliche �berlebensvorteil von 30% bewirkt. In Tierstudien wurde gezeigt, dass Ald und nicht Ang II das Hauptpathogen bei der Entwicklung einer thrombotischen Mikroangiopathy der Niere ist. In vitro konnten wir zeigen, dass die fr�he Signaltransduktion vom Ang II vom Ald und dem MR abh�ngig ist, Mittlerproteine f�r dieses Ph�nomen sind bis heute nicht bekannt. Im Rahmen dieses Projektes sind folgende Untersuchungen geplant: 1) Im verschiedenen Tiermodellen soll die Rolle vom zirkulierenden und lokal produzierten Ald bei der Entstehung des prim�r Ang II induzierten, des isch�mischen und des immunologischen Endorganschadens verglichen werden. 2) In verschiedenen MR-konditionellen Knockoutm�usen soll die Bedeutung des MR ebenfalls untersucht werden. Zus�tzlich wird in vitro die Gef��reagibilit�t der unterschiedlichen Mausst�mme getestet. 3) In Zellen, welche weder einen MR noch einen Ang II Rezeptor haben soll durch Transfektion beider Rezeptoren die Funktion des MR in der Ang II und der Ald induzierten Signaltransduktion und Zellmigration untersucht werden. Wir wollen mit den beschriebenen Experimenten die Ald abh�ngige Physiologie und Pathophysiologie besser verstehen lernen und weitere notwendige Indikationen f�r den therapeutischen Einsatz der MR-Blocker aufzeigen.  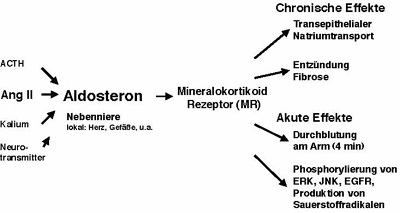 Mazak I, Fiebeler A, Muller DN, Park J-K, Shagdarsuren E, Lindschau C, Dechend R, Pilz B, Haller H, Luft FC. Aldosterone potentiates angiotensin II-induced signaling in vascular smooth muscle cells. Circulation 2004;109:2792-2800. Fiebeler A, Schmidt F, M�ller DN, Park J-K, Dechend R, Bieringer M, Shagdarsuren E, Breu V, Haller H, Luft FC: Mineralocorticoid receptor affects AP-1 and NF-κB activation in angiotensin II-induced cardiac injury. Hypertension 2001; 37:787-93. Fiebeler A, Nussberger J, Shagdarsuren E, Rong S, Hilfenhaus G, Al-Saadi N, Dechend R, Wellner M, Meiners S, Maser-Gluth C, Jeng AY, Webb RC, Luft FC, Mueller DN. An Aldosterone Synthase Inhibitor Ameliorates Angiotensin II-induced Organ Damage. Circulation. 2005; in press.  Angiotensin II-induzierte Entz�ndungsreaktionen und ihre Kontrolle durch P450-abh�ngige Metabolite mehrfach unges�ttigter Fetts�uren. Project Leader: D. N. M�ller, J. Theuer in collaboration with W-H Schunck, Max-Delbr�ck Center, Berlin Funding: DFG Dieses Projekt befa�t sich mit der Entstehung chronischer Entz�ndungsreaktionen wie sie bei Ang II-induziertem Bluthochdruck auftreten und dabei zur Sch�digung von Blutgef��en und Endorganen beitragen. Ausgangspunkt sind eigene Vorarbeiten an einem transgenen Rattenmodell, bei dem erh�hte Ang II-Konzentrationen eine pro-inflammatorische Signalkaskade in der Niere ausl�sen. Als Ursache f�r den �bergang in einen pathologischen Entz�ndungsprozess vermuten wir den gleichzeitigen Ausfall eines anti-inflammatorischen Signaltransduktionsweges, welcher auf der P450-abh�ngigen Bildung von 11,12-Epoxyeicosatriens�ure (11,12-EET) beruht. Zur �berpr�fung dieser Hypothese sollen folgende Fragestellungen bearbeitet werden: (1) Ver�nderungen in der Expression und Aktivit�t der beteiligten P450 Isoformen, (2) die Wirkung von 11,12-EET und anderer P450-abh�ngiger Metabolite mehrfach unges�ttigter langkettiger Fetts�uren auf die Ang II-induzierte Aktivierung des pro-inflammatorischen Transkriptionsfaktors NF-κB und (3) die m�gliche Rolle der P450-Metabolite als aktivierende Liganden des anti-inflammatorisch wirkenden Transkriptionsfaktors PPAR Γ. Und (4) Rolle von CYP-abh�ngigen Eicosanoiden bei der Ang II-induzierten Signaltransduktion in Gef��muskelzellen. 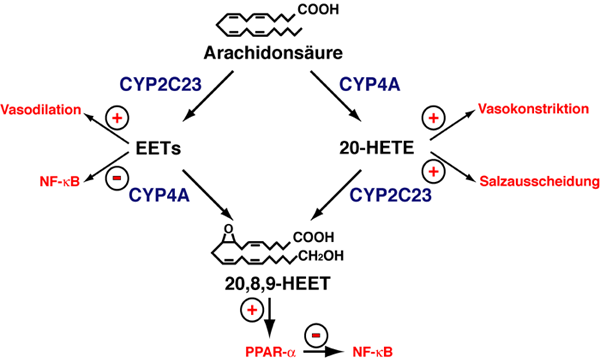 Kaergel E, M�ller DN, Honeck H, Theuer J, Mullally A, Luft FC, Schunck W-H: Cytochrome P450-dependent renal metabolism of arachidonic acid in a rat model of angiotensin II induced hypertension and end-organ damage. Hypertension 2002;40:273-9. M�ller DN, Theuer J, Shagdarsuren E, Kaergel E, Honeck H, Park J-K, Markovic M, Barbosa-Sicard E, Dechend R, Wellner M, Kirsch T, Fiebeler A, Haller H, Luft FC, Schunck W-H. A PPAR Γ activator restores renal CYP2C23 activity and protects from Ang II-induced renal injury. Am J Pathol. 2004;164:521-32. Theuer J, Shagdarsuren E, Muller DN, Kaergel E, Honeck H, Park J-K, Fiebeler A, Dechend R, Haller H, Luft FC, Schunck W-H: Eicosapentaenoic acid supplementation, but not iNOS blockade, protects from angiotensin II-induced renal damage. Kid Int 2005;67:248-58.  |